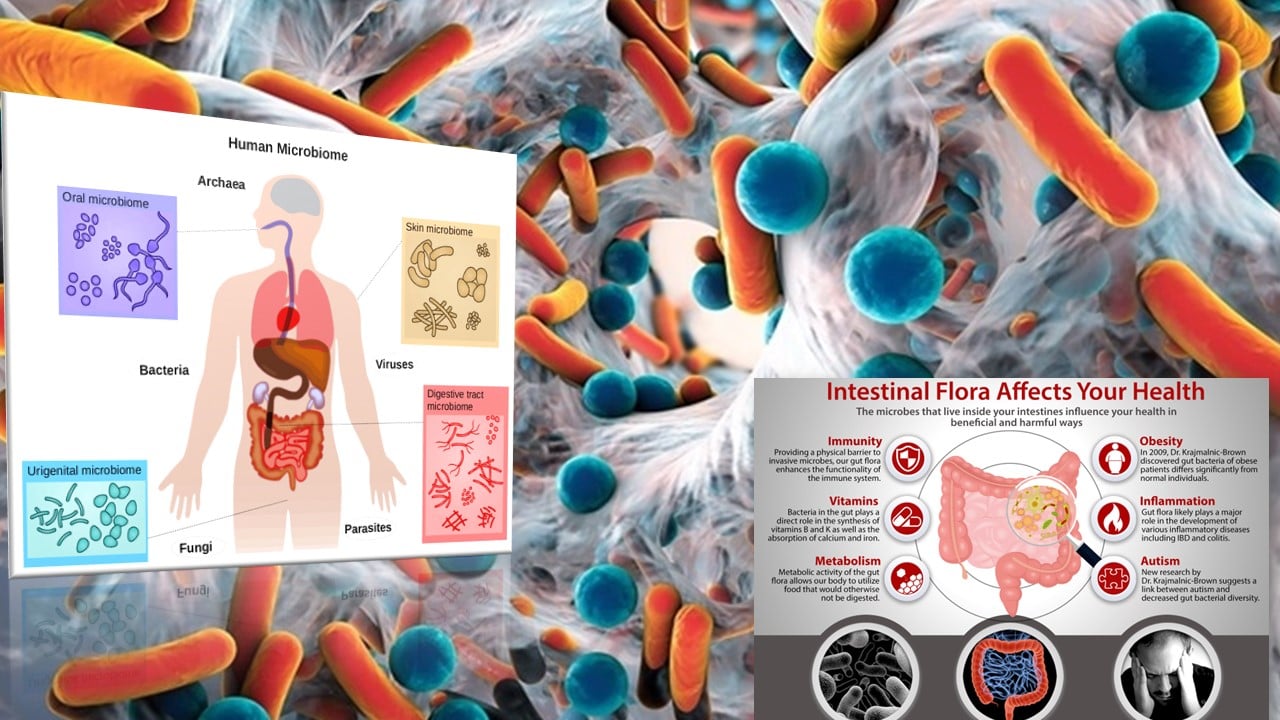
10 ก.ค. 2566 – ศูนย์จีโนมทางการแพทย์ คณะแพทยศาสตร์ โรงพยาบาลรามาธิบดี โพสต์ข้อความผ่านเฟซบุ๊กว่า งานวิจัยล่าสุดชี้ว่าชนิดและจำนวนจุลินทรีย์ในลำไส้ของคนก่อนเกิดภาวะสมองเสื่อม “อัลไซเมอร์” มีความแตกต่างไปจากคนที่มีสุขภาพดี
ศูนย์จีโนมทางการแพทย์ ใช้การตรวจรหัสพันธุกรรมจีโนมของจุลชีพด้วยตัวตรวจตามจำเพาะ (specific probes) เพื่อติดตามชนิดและปริมาณของกลุ่มจุลชีพสำคัญในลำไส้ของประชากรไทย 48 สายพันธุ์ เพื่อตรวจหาความไม่สมดุลระหว่างจุลินทรีย์ที่ ‘ดี’ และ ‘ไม่ดี’ ในลำไส้ (Dysbiosis) อันส่งผลต่อสุขภาวะของแต่ละบุคคล
ทีมวิจัยจากคณะแพทยศาสตร์มหาวิทยาลัยวอชิงตัน (Washington University School of Medicine) ในสหรัฐอเมริกา พบว่าบรรดาจุลชีพในลำไส้ของกลุ่มคนที่ตรวจพบสมองเสื่อมจากการสแกนสมองทั้งใน “กลุ่มที่ยังไม่แสดงอาการ”และ “กลุ่มที่แสดงอาการอัลไซเมอร์” มีชนิดและจำนวนของจุลินทรีย์แตกต่างจากกลุ่มบุคคลที่มีสุขภาพดี โดยตีพิมพ์ผลงานวิจัยในหัวข้อ “ชนิดและปริมาณของจุลินทรีย์ในลำไส้อาจเป็นตัวบ่งชี้ถึงโรคอัลไซเมอร์ได้ก่อนแสดงอาการ (Gut microbiome composition may be an indicator of preclinical Alzheimer’s disease) ในวารสาร Science Translational Medicine (https://www.science.org/doi/10.1126/scitranslmed.abo2984)
โดยงานวิจัยแสดงให้เห็นว่าในกลุ่มคนที่พบการเสื่อมของสมองในระยะแรกด้วยการสแกนสมองด้วยเทคโนโลยี PET และ MRI scan โดยที่ยังไม่มีอาการทางคลินิกของอาการเสื่อมทางสมองในด้าน ความจำ, ความสนใจ, การรับรู้, ภาษา และการแก้ไขปัญหาปรากฏขึ้น โดยพบว่ากลุ่มคนเหล่านี้มีแบคทีเรียในลำไส้ที่แตกต่างกันเมื่อเทียบกับคนที่มีสุขภาพดีอย่างมีนัยสำคัญ
การค้นพบนี้ตีพิมพ์ในวารสาร Science Translational Medicine เมื่อวันที่ 14 มิถุนายน 2566 ชี้ให้เห็นถึงแสงสว่างปลายอุโมงค์ในการวินิจฉัยหรือการรักษาใหม่ๆ ที่มุ่งเป้าไปที่จุลินทรีย์ในลำไส้สำหรับโรคอัลไซเมอร์
นักวิจัยเสนอว่าอาจเป็นไปได้ที่จะระบุบุคคลที่มีความเสี่ยงสูงต่อการเกิดภาวะสมองเสื่อมโดยการวิเคราะห์ชุมชนจุลลินทรีย์หรือไมโครไบโอม(microbiome) ในลำไส้ของพวกเขา นอกจากนี้ยังสามารถเลือกใช้การรักษาที่มุ่งเป้าปรับเปลี่ยนไมโครไบโอม หรือการใช้ยาบางชนิดเพื่อป้องกัน ชะลอ หรือรักษาโรคอัลไซเมอร์ ก่อนที่จะมีอาการรุนแรงแก้ไขไม่ได้
อย่างไรก็ดีขณะนี้ยังไม่ชัดเจนว่า “การเปลี่ยนแปลงทางพยาธิสภาพในสมอง ส่งผลให้เกิดการเปลี่ยนแปลงของไมโครไบโอมในลำไส้” หรือ “ไมโครไบโอมในลำไส้ส่งผลให้เกิดการเปลี่ยนแปลงพยาธิสภาพในสมอง อันก่อให้เกิดโรคอัลไซเมอร์”
อนึ่งหากเป็นอย่างแรกคือการเปลี่ยนแปลงทางพยาธิสภาพในสมอง ส่งผลให้มีการเปลี่ยนแปลงของไมโครไบโอมในลำไส้ เราอาจสามารถใช้ชนิดและปริมาณของไมโครไบโอมในลำไส้เป็นตัวช่วยบ่งชี้การเกิดอัลไซเมอร์ก่อนแสดงอาการ และรักษาด้วยยาตั้งแต่ระยะแรกเริ่ม
แต่หากไมโครไบโอมในลำไส้ส่งผลให้เกิดการเปลี่ยนแปลงพยาธิสภาพในสมอง เราสามารถพัฒนาการป้องกันโรคอัลไซเมอร์โดยการเปลี่ยนแปลงชนิดและจำนวนไมโครไบโอมในลำไส้ เช่น การรับประทานพรีไบโอติก (prebiotics) และ โปรไบโอติก (Probioitcs) ที่จำเพาะ
พรีไบโอติกเป็นไฟเบอร์ที่ย่อยไม่ได้ซึ่งทำหน้าที่เป็นอาหารของแบคทีเรียที่มีประโยชน์ในลำไส้ พรีไบโอติกส่งเสริมการเจริญเติบโตของแบคทีเรียที่ดีซึ่งสามารถปรับปรุงการย่อยอาหารและสุขภาพของลำไส้โดยรวม พรีไบโอติกพบได้ในอาหารบางชนิดและสามารถรับประทานได้จากอาหารเสริม
โปรไบโอติกเป็นจุลินทรีย์ที่มีประโยชน์ต่อร่างกายหากบริโภคในปริมาณที่เพียงพอ อันจะช่วยส่งเสริมสุขภาพทางเดินอาหารและปรับสมดุลของจุลินทรีย์ในลำไส้ โปรไบโอติกสามารถปรับปรุงการย่อยอาหาร การดูดซึมสารอาหาร และสุขภาพของลำไส้โดยรวม โปรไบโอติกมีอยู่ในอาหารและอาหารเสริม และสายพันธุ์ทั่วไป ได้แก่ แลคโตบาซิลลัสและบิฟิโดแบคทีเรียม
ก่อนหน้านี้เป็นที่ทราบกันดีว่าไมโครไบโอมในลำไส้ของผู้ป่วยอัลไซเมอร์มีทั้งชนิดและปริมาณที่แตกต่างจากผู้ที่มีสุขภาพดี แต่ยังไม่มีการวิจัยสำรวจชนิดและปริมาณไมโครไบโอมใน “ระยะก่อนมีอาการอัลไซเมอร์”
ในช่วงระยะแรกของอัลไซเมอร์ ซึ่งอาจกินเวลาตั้งแต่สองทศวรรษขึ้นไป มีการสะสมของโปรตีนอะไมลอยด์ เบตาและโปรตีนทาว (Tau) ในสมอง แต่ยังไม่มีสัญญาณของการเสื่อมของระบบประสาทหรือการรับรู้ที่ลดลง
นักวิจัยประเมินอาสาสมัครเข้าร่วมโครงการ 164 คนที่มีสุขภาพดี; ประมาณหนึ่งในสาม (49) มีอาการสมองเสื่อมในระยะแรกที่ยังไม่แสดงอาการ โดยพบว่าแบคทีเรียในลำไส้ระหว่างคนที่มีสุขภาพดีและผู้ที่เป็นโรคอัลไซเมอร์ระยะก่อนแสดงอาการ (พรีคลินิก) มีความแตกต่างกันอย่างเห็นได้ชัด ความแตกต่างเหล่านี้มีความสัมพันธ์กับระดับของโปรตีนแอมีลอยด์และโปรตีนทาว (Tau) แต่ยังไม่พบความเกี่ยวข้องกับการเสื่อมของระบบประสาท
การค้นพบนี้ชี้ให้เห็นถึงศักยภาพของไมโครไบโอมในลำไส้ที่อาจใช้เป็นเครื่องมือคัดกรองโรคอัลไซเมอร์ระยะแรก โดยใช้ตัวอย่างเป็นอุจจาระที่เก็บได้ง่ายไม่ต้องเจาะเลือด
ทีมวิจัยวางแผนติดตามผลต่อไปอีก 5 ปี เพื่อพิจารณาว่าความแตกต่างของไมโครไบโอมในลำไส้เป็นต้นเหตุให้เกิดโรคอัลไซเมอร์หรือเป็นผลมาจากโรคอัลไซเมอร์ระยะแรกส่งผลให้ไมโครไบโอมในลำไส้เปลี่ยนแปลงไป หากพบความเชื่อมโยงและเป็นสาเหตุของโรคอย่างมีนัยสำคัญ การรักษาในอนาคตอาจมุ่งเน้นไปที่การส่งเสริมแบคทีเรีย “ดี” หรือกำจัดแบคทีเรีย “ไม่ดี” ในลำไส้
ไมโครไบโอมหมายถึงจุลินทรีย์ทั้งหมด รวมถึงแบคทีเรีย ไวรัส เชื้อรา และโปรโตซัว ซึ่งอาศัยอยู่ภายในร่างกายมนุษย์ จุลินทรีย์เหล่านี้ส่วนใหญ่อาศัยอยู่ในลำไส้ มีความสำคัญต่อการรักษาสภาวะสมดุลและสุขภาพโดยรวม ไมโครไบโอมสามารถส่งผลต่อร่างกายและสุขภาพของคุณได้ด้วยวิธีต่อไปนี้:
1.การย่อยอาหาร: ไมโครไบโอมในลำไส้ช่วยในการสลายสารประกอบในอาหารที่ซับซ้อนซึ่งเซลล์ของมนุษย์ไม่สามารถย่อยได้ เช่น เส้นใยบางชนิด พวกมันสามารถสลายสารเหล่านี้ให้เป็นกรดไขมันสายสั้น เช่น บิวทิเรต โพรพิโอเนต และอะซีเตต ซึ่งสามารถให้พลังงานแก่เซลล์ของเราได้
2.การปรับระบบภูมิคุ้มกัน: ไมโครไบโอมมีบทบาทสำคัญในการสร้างและควบคุมระบบภูมิคุ้มกัน ในการพัฒนาการตอบสนองของภูมิคุ้มกันที่ดีต่อสุขภาพ ช่วยให้ร่างกายของคุณแยกแยะระหว่างผู้บุกรุกที่ไม่เป็นอันตรายและอาจเป็นอันตรายได้
3.สุขภาพจิต: การวิจัยใหม่ชี้ให้เห็นว่าไมโครไบโอมอาจส่งผลต่อสุขภาพจิต การศึกษาบางชิ้นพบความสัมพันธ์ระหว่างการเปลี่ยนแปลงของจุลินทรีย์ในลำไส้กับภาวะสุขภาพจิต เช่น ความวิตกกังวล ภาวะซึมเศร้า และความผิดปกติทางพัฒนาการทางระบบประสาท รวมถึงออทิสติก และอาจรวมถึงอาการอัลไซเมอร์
4.การควบคุมน้ำหนัก: องค์ประกอบของไมโครไบโอมในลำไส้มีความเชื่อมโยงกับน้ำหนักตัว โดยแบคทีเรียบางชนิดพบได้บ่อยในคนที่เป็นโรคอ้วนมากกว่าคนที่ไม่อ้วน การศึกษาบางชิ้นแนะนำว่าแบคทีเรียเหล่านี้อาจส่งผลต่อน้ำหนักโดยส่งผลต่อวิธีที่เราเผาผลาญอาหารและดูดซึมสารอาหาร
5.สุขภาพเมตาบอลิซึม: ไมโครไบโอมในลำไส้มีส่วนเกี่ยวข้องกับโรคเมตาบอลิซึมหลายชนิด รวมถึงเบาหวานชนิดที่ 2 และโรคไขมันพอกตับ การเปลี่ยนแปลงของไมโครไบโอมในลำไส้อาจส่งผลต่อการเผาผลาญของร่างกายและความไวของอินซูลิน
6.สุขภาพหัวใจ: ไมโครไบโอมในลำไส้สามารถส่งผลต่อสุขภาพหัวใจโดยส่งผลต่อปัจจัยต่างๆ เช่น การอักเสบและระดับคอเลสเตอรอล แบคทีเรียในลำไส้บางชนิดสามารถผลิตสารที่ส่งผลต่อสุขภาพของหัวใจ เช่น TMAO (trimethylamine N-oxide) ซึ่งเชื่อมโยงกับหลอดเลือด
7.สุขภาพผิว: การวิจัยล่าสุดชี้ให้เห็นว่าไมโครไบโอมของผิวหนังมีบทบาทสำคัญในสภาวะต่างๆ เช่น สิว โรคสะเก็ดเงิน และโรคเรื้อนกวาง
ศูนย์จีโนมฯ เลือกตรวจกลุ่มแบคทีเรีย 48 สายพันธุ์ ด้วยเทคโนโลยี “Luminex” ในการวัดความไม่สมดุลของชุมชนจุลินทรีย์ในลำไส้ที่ส่งผลต่อสุขภาวะ (Dysbiosis) อันก่อให้เกิดการเจ็บป่วยได้อย่างหลากหลาย โดยใช้เม็ดบีด (bead) เล็กๆ 100 ชนิดที่สามารถเรื่องแสงแตกต่างกันได้ถึง 100 เฉดสี โดยที่เม็ดบีดจะติดโมเลกุลพิเศษที่สามารถจับกับจีโนมของเชื้อจุลินทรีย์แต่ละชนิดในตัวอย่างได้อย่างจำเพาะ จากนั้นนำไปวัดการเรืองแสงด้วยเครื่องที่เรียกว่าโฟลไซโตมิเตอร์ที่สามารถอ่านเม็ดบีดเรืองแสงได้ถึง 100 เฉดสี และผลจากการวิเคราะห์เฉดสีจะช่วยบอกเราว่ามีเชื้อจุลินทรีย์อะไร มีปริมาณเท่าไรในตัวอย่างส่งตรวจได้อย่างถูกต้อง ไม่คลาดเคลื่อน เนื่องจากต้องนำผลการตรวจสอบมาเปรียบกับการตรวจในครั้งก่อนเป็นระยะ (monitoring) ในขณะที่หากใช้เทคโนโลยีการถอดรหัสพันธุกรรมขั้นสูง หรือ next generation sequencing/NGS จะมีความคลาดเคลื่อนสูงกว่า สังเกตจากการทดสอบตัวอย่างเดียวกันซ้ำด้วยเทคนิค NGS จะให้ผลของชนิดและจำนวนของจุลินทรีย์ที่คลาดเคลื่อนไม่ตรงกัน (Multicenter quality assessment of 16S ribosomal DNA-sequencing for microbiome analyses reveals high inter-center variability https://pubmed.ncbi.nlm.nih.gov/27052158/)
ดังนั้นการตรวจกลุ่มจุลินทรีย์ด้วยเทคโนโลยี Luminex จึงได้ใบรับรอง “CE-IVD” หรือ “Conformité Européenne – In Vitro Diagnostic Devices” ให้ใช้ได้กับตัวอย่างของคนปรกติหรือจากคนไข้ในโรงพยาบาลในยุโรปเพื่อตรวจสอบสภาวะ “Dysbiosis”
Dysbiosis หมายถึงความไม่สมดุลตามธรรมชาติของชุมชนจุลินทรีย์ที่อาศัยอยู่ในสภาพแวดล้อมหนึ่งๆ ซึ่งใช้กันมากที่สุดในการอ้างอิงถึงจุลินทรีย์ในลำไส้
จุลินทรีย์ในลำไส้ประกอบด้วยจุลินทรีย์นับล้านล้านตัว รวมถึงแบคทีเรีย ไวรัส เชื้อรา และสิ่งมีชีวิตเซลล์เดียวอื่นๆ ที่อาศัยอยู่ในระบบทางเดินอาหารและมีบทบาทสำคัญในการย่อยอาหาร การทำงานของระบบภูมิคุ้มกัน และสุขภาพโดยรวม
Dysbiosis อาจเกิดจากปัจจัยต่างๆ เช่น การรับประทานอาหารที่ไม่ดี ความเครียด ขาดการออกกำลังกาย การใช้ยาปฏิชีวนะ และอิทธิพลของสิ่งแวดล้อมอื่นๆ
ความไม่สมดุลนี้อาจนำไปสู่การลดลงของจุลินทรีย์ที่มีประโยชน์และการเพิ่มขึ้นของจุลินทรีย์ที่อาจเป็นอันตราย ซึ่งอาจนำไปสู่ปัญหาสุขภาพต่างๆ ปัญหาสุขภาพบางอย่างเหล่านี้ ได้แก่ โรคลำไส้อักเสบ (IBD) โรคลำไส้แปรปรวน (IBS) โรคอ้วน โรคเมตาบอลิซึม และแม้แต่ความผิดปกติทางสุขภาพจิต เช่น ความวิตกกังวลและภาวะซึมเศร้า รวมถึง “อัลไซเมอร์”
การฟื้นฟูจุลินทรีย์ในลำไส้ให้สมดุลเป็นสิ่งจำเป็นสำหรับการรักษาสุขภาพโดยรวม ซึ่งสามารถทำได้โดยการเปลี่ยนแปลงวิถีชีวิต (ปรับเปลี่ยนพฤติกรรม) ซึ่งรวมถึงอาหารเพื่อสุขภาพที่อุดมด้วยไฟเบอร์ การออกกำลังกายเป็นประจำ การจัดการความเครียด และการใช้ยาปฏิชีวนะอย่างเหมาะสม ในบางกรณี โปรไบโอติกและพรีไบโอติกอาจมีประโยชน์ในการส่งเสริมสมดุลของจุลินทรีย์ในลำไส้.
ข่าวที่เกี่ยวข้อง
ศูนย์จีโนมฯ ถอดรหัสทำไมหลังสงกรานต์ไวรัสตับอักเสบเอระบาดหนัก!
เพจ Center for Medical Genomics ของศูนย์จีโนมทางการแพทย์ คณะแพทยศาสตร์
เปิดเบื้องหลัง! มฤตยูเงียบในทุ่งนา 'โรคไข้ดิน'
เพจ "Center for Medical Genomics" ของศูนย์จีโนมทางการแพทย์ คณะแพทยศาสตร์โรงพยาบาลรามาธิบดี โพสต์ข้อความเรื่อง "แกะรอยมฤตยูเงียบในทุ่งนา: เบื้องหลัง ‘โรคไข้ดิน’ และความหวังใหม่จากมุกดาหารโมเดล" โดยระบุว่า
ซีดีซีสหรัฐเผยโฉม BA.3.2 สายพันธุ์โควิดที่ซ่อนตัวเก่งที่สุด!
ศูนย์จีโนมทางการแพทย์ คณะแพทยศาสตร์ โรงพยาบาลรามาธิบดี มหาวิทยาลัยมหิดล
ศูนย์จีโนมฯ เตือน 2 ไวรัสภัยเงียบที่กำลังเคาะประตูบ้านเรา!
เพจศูนย์จีโนมทางการแพทย์ คณะแพทยศาสตร์ โรงพยาบาลรามาธิบดี มหาวิทยาลัยมหิดล
'งีบกลางวัน' บ่อยและนาน เร่งสมองเสื่อม!
ศ.นพ.ธีระวัฒน์ เหมะจุฑา ประธานศูนย์ความเป็นเลิศ ด้านการแพทย์บูรณาการและสาธารณสุข และที่ปรึกษาวิทยาลัยการแพทย์แผนตะวันออก มหาวิทยาลัยรังสิต
กินเหล้าหัวราน้ำ! กระทบตับ ส่วนที่ป้องกันอัลไซเมอร์
ศ.นพ.ธีระวัฒน์ เหมะจุฑา ศาสตราจารย์เชี่ยวชาญทางอายุรกรรมและสมอง ประธานศูนย์ความเป็นเลิศการแพทย์บูรณาการและสาธารณสุข และที่ปรึกษาวิทยาลัยการแพทย์แผนตะวันออก มหาวิทยาลัยรังสิต

